HIDRONIDONA PARA LA FIBROSIS DE LA HEPATITIS B
- Escrito por Dr. Jorge Luis Poo
- Publicado en Hepatitis virales

La HIDRONIDONA es un nuevo fármaco, derivado de la pirfenidona, que segun los investigadores fue creado para reducir su potencial toxicidad. Según la poca información disponible, la hidronidona contiene una modificación estructural de la molecula original de pirfenidona. En estudios experimentales con roedores, la hidronidona reduce la expresión del factor de crecimiento transformante tipo 1 (abreviado como TGF beta1) lo cual disminuye la producción de hidroxiprolina, un constituyente de la colágena y, por lo tanto, reduce la progresión de la fibrosis hepática en el ratón con daño por tetracloruro de carbono. Estos resultado tan prometedores permitieron que se avanzara a estudios en el ser humano, demostrando inicialmente la seguridad de su administración en voluntarios sanos (estudios de fase farmacológica 1). El estudio publicado incluyó a 88 sujetos divididos en diferentes grupos con dosis variables entre 180 y 360 mg, por día, demostrando una adecuada tolerancia.
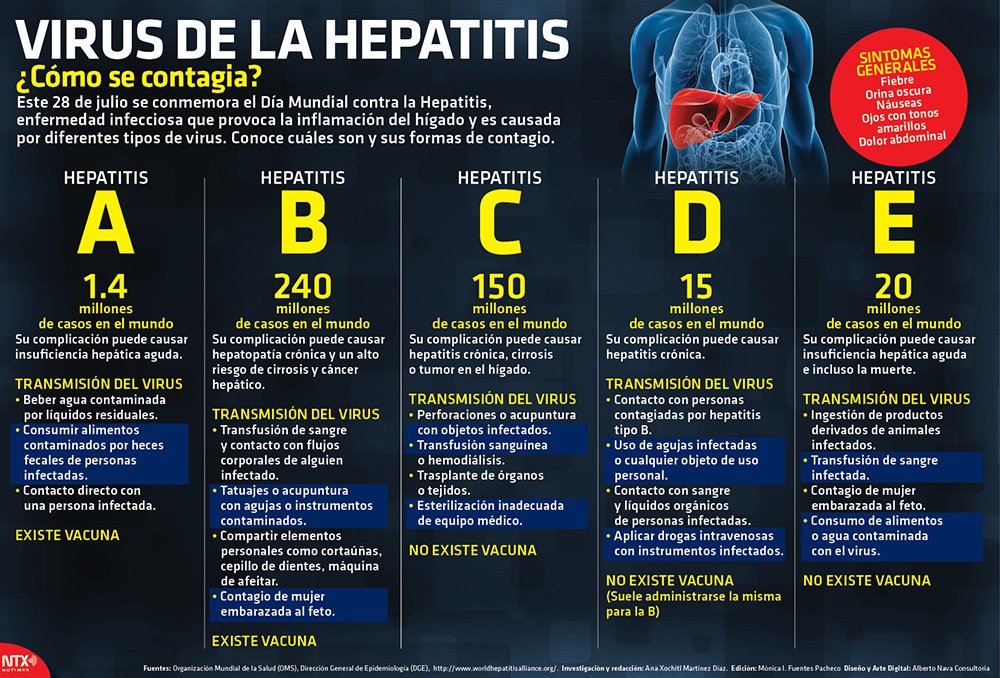
La hepatitis B es un gran problema de salud a nivel mundial. La hepatitis B es una infección vírica del hígado que puede dar lugar tanto a un cuadro agudo como a una enfermedad crónica. El virus de la hepatitis B se transmite más comúnmente de madre a hijo durante el parto, así como a través del contacto con sangre u otros líquidos corporales durante las relaciones sexuales con una pareja infectada, las inyecciones sin suficiente protección frente a riesgos o la exposición a instrumentos afilados durante la atención de salud o en el entorno comunitario. La OMS estima que 296 millones de personas padecían infección crónica por el virus de la hepatitis B en 2019, y cada año se producen 1,5 millones de nuevas infecciones. En 2019, la hepatitis B causó unas 820 000 muertes, principalmente por cirrosis o carcinoma hepatocelular (cáncer primario del hígado).
El Doctor Xiaobo Cai y el Profesor Lungen Lu así como diversos colaboradores del Departamento de Gastroenterología del Shangai General Medical Hospital,en China, en colaboración con el Dr. Ying Luo de la Continent Pharmaceuticals, de Beijing China, recientemente publicaron un artículo en la revista Clinical Gastroenterology and Hepatology, en la cual presentan su experiencia con este nuevo fármaco, en un estudio de fase 2 farmacológica, en pacientes con hepatitis crónica viral B.
Objetivo del estudio:
Evaluar la seguridad y eficacia de diversas dosis del fármaco antifibrótico hidronidona en pacientes con fibrosis por hepatitis crónica viral B.
Metodología:
Se incluyeron pacientes en 8 centros clínicos de China que cumplieron con los siguientes criterios de elección:
- Edad entre 18 y 65 años
- Historia de hepatitis B, con antigeno de superficie positivo por lo menos 6 meses
- Niveles de transaminasas menores de 8 veces el límite superior de lo normal
- Con fibrosis hepática significativa d, de acuerdo a biopsia hepática, con puntaje de Ishak mayor de 3 sobre 6.
- Niveles de DNA positivos (mayores de >2.0 104 IU/mL) en pacientes con antigeno e positivo
- Niveles de DNA positivos (mayores de >2.0 103 IU/mL) en pacientes con antigeno e negativo
Sin tratamiento antiviral previo
Los criterios de exclusión fueron los siguientes:
- Cirrosis hepática descompensada
- Otras causas de enfermedad hepática crónica
- Hemorragia digestiva en los 3 meses previos a la inclusión
- Enfermedades cardiovascular, pulmonar, renal, endocrina, neurologica, hematológica, o psiquiatrica asociadas.
- Cancer hepático
- Tiempo de protrombina menor del 50%
- Bilirrubina mayor de 3 veces el valor límite de lo normal
- Sospecha de trombosis de a vena porta (vena menos de 1.2 cm segun ultrasonido)
- Indice de masa corporal mayor de 30 para eliminar la posibilidad de enfermedad metabólica hepática asociada.
Los pacientes fueron asignados al azar a recibir las siguientes opciones de tratamiento:
- Placebo
- Hidronidona 180 mg/día (una tableta de 60 mg, tres veces al día)
- Hidronidona 270 mg/día (no se especifica el regimen, peros suponemos que fue 90 mg, tres veces al día)
- Hidronidona 360 mg/día (dos tabletas de 60 mg, tres veces al día)
Todos los pacientes recibieron 0.5 mg del farmaco antiviral llamado entecavir cada día, a lo largo del estudio.
Todos los pacientes debían aceptar dos biopsias hepáticas, la basal y al terminar un año de tratamiento. La biopsia debía ser de al menos 1 cm de longitud y contener al menos 6 espacios porta para análisis histopatólogico por tres Patólogos independientes, quienes revisaron las biopsias en forma ciega, utilizando la escala de Ishak que considera 6 nivles de fibrosis. Se evaluó también la inflamación. Se evaluó la concordancia entre los 3 patólogos y se buscó un acuerdo en su evaluación en los casos discordantes. Los criterios de eficacia fueron los siguientes:
- Disminución de al menos 1 punto en el puntaje de Ishak (objetivo primario) en las 52 semanas de tratamiento.
- Fibrosis en regresión: en casos de reducción mayor a un punto de Ishak, en 52 semanas.
- Fibrosis en progresión: en casos de incremento mayor a un punto de Ishak, en 52 semanas.
- Regresión de la cirrosis: en casos de reducción superior a 2 puntos en el puntaje de Ishak, a las 52 semanas.
- Progresión a la cirrosis: cuando alguien con puntajes menors de 4, alcanza un puntaje 6 de Ishak, a las 52 semanas.
Todos los pacientes fueron evaluados cada 4 semanas, durantes 52 semanas. Se evaluaron todos los eventos adversos. El estudio se realizó entre el 25-Jun-2015 y el 5-Sep-2019. Se calculó un tamaño ideal de la población de 136 sujetos, 36 por cada grupo de estudio. Considerando la posibilidad de un alto novel de pérdidas de sujetos por la necesidad de 2 biopsias, se decidió intentar reclutar a 240 sujetos. Sin embargo, para 2019 solo se logró reclutar a 168 sujetos.
Resultados:
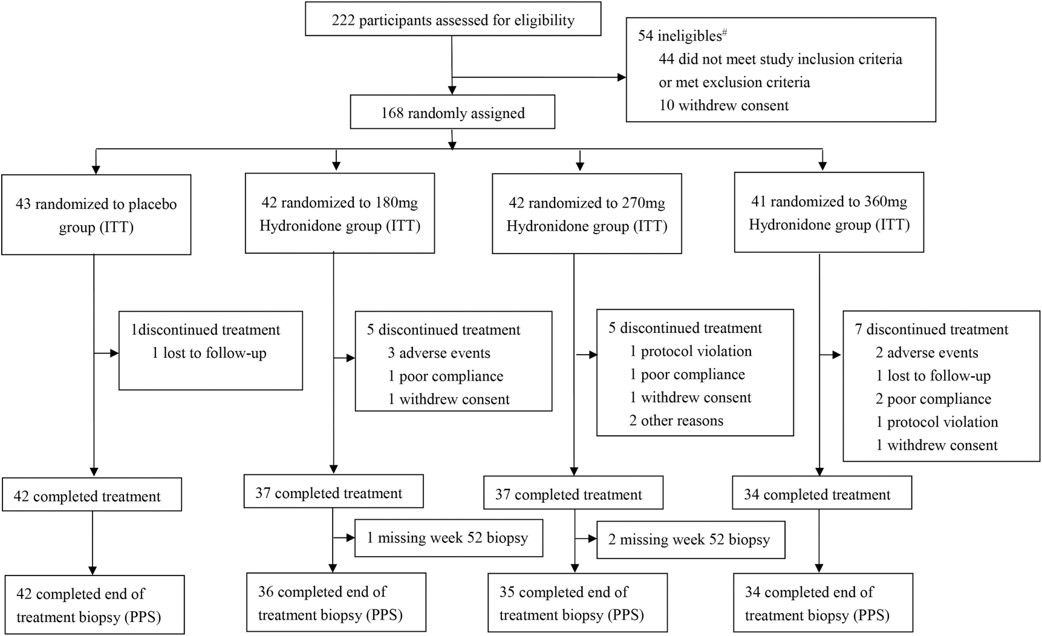
Durante el período de reclutamiento se lograron reclutar a 222 sujetos, pero 10 de ellos retiraron el consentimiento. Durante la fase de tratamiento algunos pacientes desertaron del estudio o bien no aceptaron la segunda biopsia. Al final se logró disponer de información en 147 pacientes (el 87.5% de los que lograron alcanzar la semanana 52 de tratamiento), 42 del grupo placebo, 36 en el grupo de 180 mg, 35 en el de 270 mg y 34 en el de 360 mg por día. Las condiciones basales de los 4 grupos eran comparables en aspectos demográficos y de magnitud del daño en fibrosis.
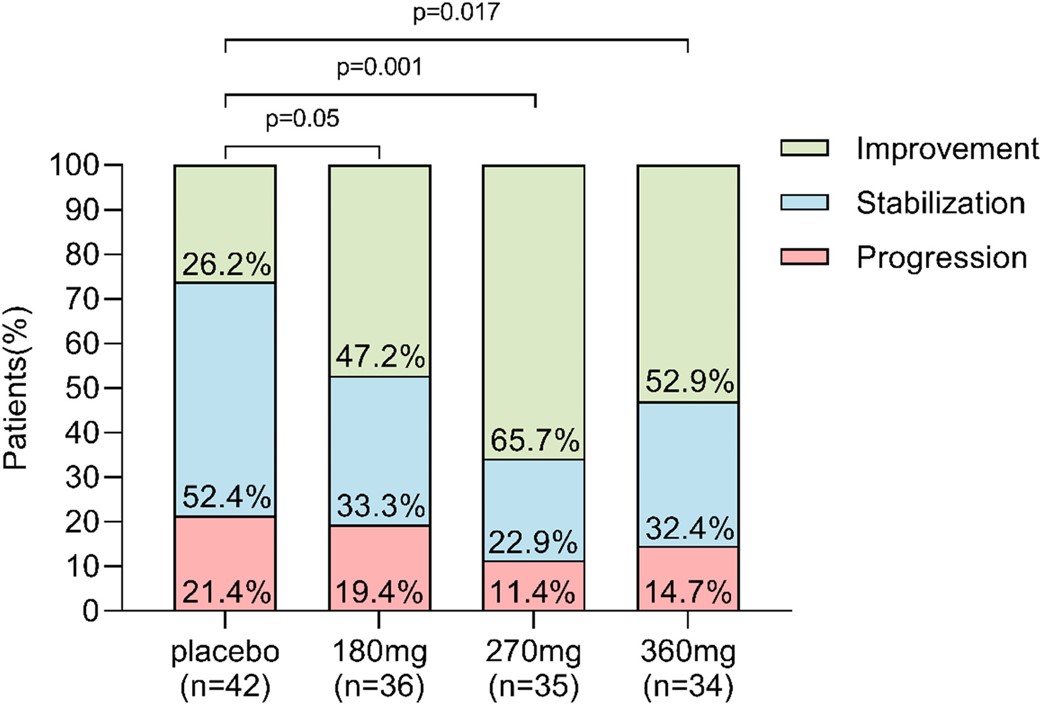
Se logró mejoría en fibrosis en las siguientes proporciones:
- En 11 pacientes (25.6%) del grupo placebo.
- En 17 pacientes (40.5%) del grupo de 180 mg por día (p de 0.12).
- En 23 pacientes (54.8%) del grupo 270 mg por día (p de 006).
- En 18 patients (43.90%) del grupo 360 mg (p de 0.08).
- La mejoría global del grupo hidronidona fue de 58 de125 pacientes (46.4%, p de .014).
- La concordancia entre patólogos fue de 0.76, lo cual segun los autores demuestra una buena concordancia.
Después del inicio del tratamiento antiviral se logró negativización del HBV DNA en 143 de los 168 sujetos (85.1% de la población), 39 de los 43 (90.7%) en el grupo placebo, 35 de los 42 (83.3%) en el grupo de 180 mg de hidronidona, 36 de 42 (85.7%) emn el grupo de 270 mg de hidronidona y en 33 de 41 (80.5%) del grupo de 360 mg de hidronidona group (p de 0.45). El alcanzar el nivel de HBV DNA indetectable se asoció a regresión de la fibrosis.
No se observó toxicidad grave o diferencias en eventos adversos entre los 4 grupos terapéuticos. Sin embargo 3 sujetos del grupo de tratamiento con hidronidona requirieron descontinuación por incremento de la transaminasas a valores mayor de 8X (8 veces el valor de lo normal) o niveles persistentemente elevados por arriba de 5X (cinco veces el valor normal) por 2 o más o más semanas. Es posible que estos incrementos de transaminasas no se debieran al medicamento sino a la propia actividad replicativa viral B.
Conclusión:
Los autores concluyen que la administración de hidronidona, junto con entecavir, demostró una eficacia antifibrótica superior al placebo en pacientes con infección crónica por virus B.
Este artículo destaca por su mensaje alentador de mejoria en la fibrosis hepática (superior al grupo placebo) en un tiempo de administración relativamente corto, gracias a la convinación del antiviral entecarvir con el antifibrótico hidronidona. Aunque en otras publicaciones se ha demostrado una mejora significativa de la fibrosis, hasta 50 a 75% a 5 años, por otros tratamientos antivirales con Adefovir, Tenofovir, la rapidez (a un año) en la respuesta de mejoría de la fibrosis es altamente estimulante.
Conviene resaltar que este trabajo se menciona la publicación del estudio mexicano del Dr. Jorge Luis Poo y colaboradores, publicado en la revista Hepatology International el año 2020, en los cuales se demuestra una mejoría de la fibrosis en 35% de los pacientes tratados con Pirfenidona, un antifibrótcio ya disponible en nuestro país, con un buen perfil de seguridad para administración a largo plazo.
Referencias:
1. Cai X, Liu X, Xie W, Ma A, Tan Y, Shang J, Zhang J, Chen C, Yu Y, Qu Y, Zhang L, Luo Y, Yin P, Cheng J, Lu L. Hydronidone for the Treatment of Liver Fibrosis Related to Chronic Hepatitis B: A Phase 2 Randomized Controlled Trial. Clin Gastroenterol Hepatol. 2022 Jul 13:S1542-3565(22)00650-4. doi: 10.1016/j.cgh.2022.05.056. Epub ahead of print. PMID: 35842120.
2. World Health Organization. WHO Global hepatitis report, 2019. WHO Global progress report on HIV, viral hepatitis, and sexually transmitted infections, 2021: https://www.who.int/es/news-room/fact-sheets/detail/hepatitis-b
3. Hadziyannis S.J. Tassopoulos N.C. Heathcote E.J. et al. Adefovir Dipivoxil 438 Study Group. Long-term therapy with adefovir dipivoxil for HBeAg-negative chronic hepatitis B for up to 5 years. Gastroenterology. 2006; 131: 1743-1751
4. Marcellin P. Gane E, Buti M, et al. Regression of cirrhosis during treatment with tenofovir disoproxil fumarate for chronic hepatitis B: a 5-year open-label follow-up study. Lancet. 2013; 381: 468-475.
5. Poo J.L., Torre A., Aguilar-Ramírez J.R., et al. Benefits of prolonged-release pirfenidone plus standard of care treatment in patients with advanced liver fibrosis: PROMETEO study. Hepatol Int. 2020; 14: 817-827


