EL HÍGADO GRASO PUEDE AFECTAR AL PÁNCREAS
- Escrito por Dra. Fernanda García Alvarado
- Publicado en Hígado graso no Alcohólico
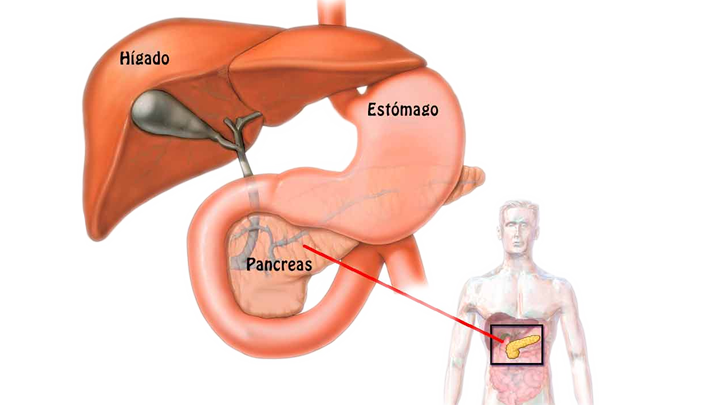
Investigadores de la Universidad de Tubingen (Alemania) han descubierto, tal y como han publicado el pasado 8 de agosto en la revista “Diabetologia and Diabetes Metab Res Rev”, que la enfermedad del hígado graso no alcohólico, también conocida como esteatosis hepática, puede causar daños a otros órganos, por ejemplo al páncreas. El hígado de estos pacientes produce cada vez más glucosa, grasas y proteínas desfavorables, así como una citocina llamada "fetuina-A", la cual se libera hacia el torrente sanguíneo y llega al páncreas. Allí produce cambios compatibles con páncreas graso que puede inducir un mal funcionamiento.
El papel de la esteatosis pancreática (pancreas con exceso de grasa) en la patogénesis de la diabetes tipo 2 está actualmente en discusión y puede depender de factores de riesgo adicionales. La acumulación de grasa en el páncreas se asocia con una reducción de la secreción de insulina en personas con intolerancia a la glucosa. Sin embargo, es controvertido si la infiltración de adipocitos y los perfiles lipídicos alterados del tejido pancreático afectan la función del islote.
Se sabe que algunas sustancias secretadas por el hígado graso (como la fetuina-A) pudieran llegar a otros órganos y provocan reacciones. No obstante, hasta ahora no se sabía qué efectos tenía esta "charla y comunicación molecular - metabólica entre el hígado y el páncreas", qué órganos son los más afectados y cuál es el "daño" causado por la hepatocina fetuína-A. Con el fin de responder a estas preguntas, los científicos analizaron la influencia de fetuina-A en el tejido adiposo pancreático. Y es que, aproximadamente un tercio del tejido adiposo pancreático se compone de células precursoras adiposas (un tipo de células madre) además de las células adiposas maduras.
Si las células adiposas pancreáticas son tratadas con fetuina-A en cultivos celulares, las células precursoras adiposas que entran en interacción con las células de los islotes, producen más mediadores de inflamación y más factores de atracción de células inmunes. En este sentido, los investigadores analizaron histológicamente muestras de tejido de 90 pacientes y encontraron que la proporción de la grasa pancreática variaba enormemente. De hecho, el número de células de defensa del sistema inmunológico (monocitos/macrófagos) se incrementó significativamente en áreas donde se habían acumulado muchas células adiposas.
Asimismo, en una cohorte de 200 sujetos con un mayor riesgo de diabetes tipo 2, el contenido de grasa pancreática se midió mediante resonancia magnética, comparando los resultados con los parámetros de la diabetes. De esta forma, los científicos encontraron que en personas que ya habían experimentado un empeoramiento en la regulación de la glucosa en sangre, el aumento de la degeneración grasa pancreática ocasionaba una secreción de insulina reducida.
Lo investigadores dicen que "el factor que conduce a cambios patológicos es la fetuina-A, que a su vez es inducido por el hígado graso". Como resultado, en lugar de que la grasa proteja al tejido como antes, el tejido adiposo en exceso ahora provoca procesos inflamatorios, lo que conduce a una restricción de la función pancreática, han explicado los expertos.
Este estudio destaca el papel de la "charla molecular y metabólica" entre las células del hígado y el páncreas que puede contribuir al desarrollo de la diabetes tipo 2. Ahora sabemos que no sólo las células beta están directamente dirigidas por factores diabetogénicos, como el palmitato y fetuina-A, sino también lo están los preadipocitos pancreáticos que se transforman en adipocitos maduros llevando a una disminución gradual de las céulas productoras de insulina.
Referencia
Gerst, F., Wagner, R., Kaiser, G., Panse, M., Heni, M., Machann, J., ... & Thiel, C. (2017). Metabolic crosstalk between fatty pancreas and fatty liver: effects on local inflammation and insulin secretion. Diabetologia, 60(11), 2240-2251.


